根据研讨会期间收集的信息,参与者指出的实施连续生物工艺HTPD的主要挑战列于表 2。此外,参与者针对所讨论的每个挑战提出了可能的解决方案。建模和微/纳米流体是这些领域进一步投资/优先考虑的主要建议,以便更轻松、更顺利地过渡到连续生物生产。这些提议的解决方案和 ICB 中的其它当前需求将被进一步讨论,特别关注 PAT 工具和单元操作的连接。
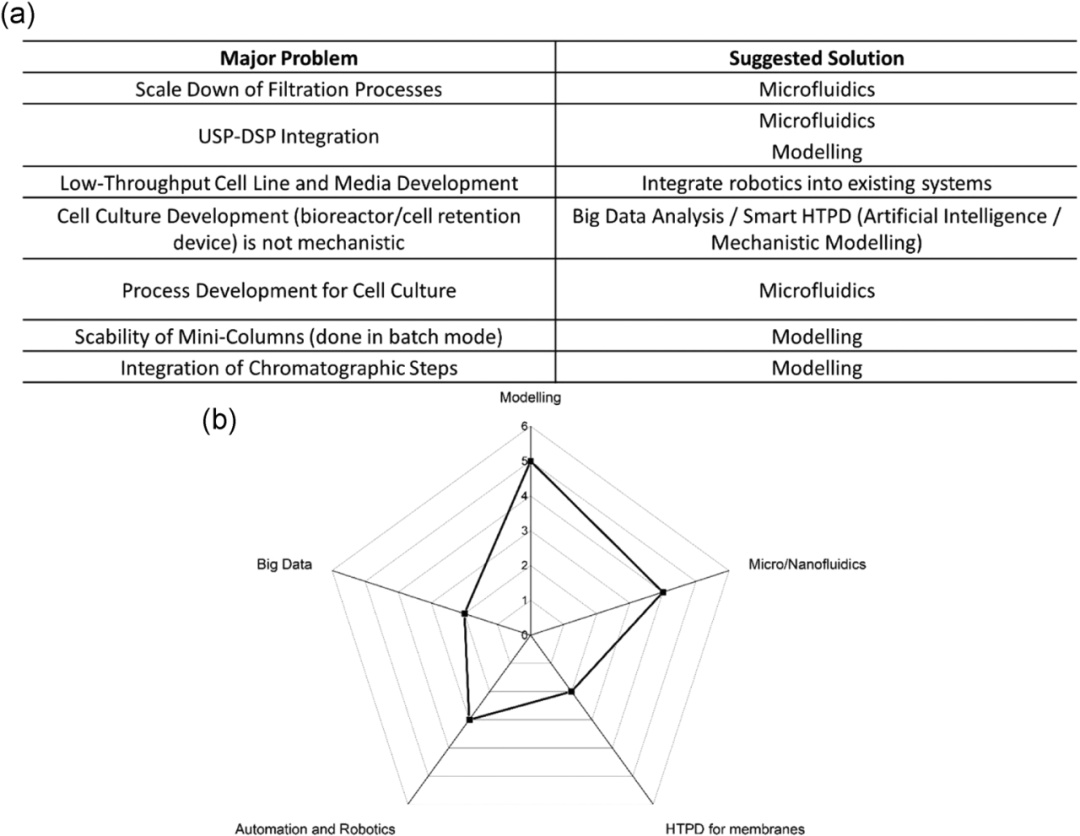
表 2 (a) 研讨会参与者指出的主要问题,以及针对 ICB 工艺开发投资/优先考虑的建议解决方案/领域;(b)参与者建议的工具摘要(只有六个小组回答了这个问题)作为 ICB 中 HTPD 当前差距/问题的解决方案
过程分析技术
PAT 被定义为“通过及时测量(即在工艺过程中)原材料和过程中材料和工艺关键质量和性能属性来设计、分析和控制生产的系统,以确保最终产品质量”。在生物制药行业实施 PAT 的最终目标是设计和开发易于理解的工艺,通过实时监控原材料或过程中的产品属性来控制工艺,从而可靠地确保最终产品的预定质量,即关键质量属性(CQA)。PAT 框架提供的、清晰的过程控制和理解支持生物制药行业采用质量源于设计 (QbD) 方法。QbD 被定义为“基于健全的科学和质量风险管理,以预先确定的目标开始,并强调对产品和工艺的理解以及过程控制的系统开发方法”。因此,PAT 实施将有助于这种系统化的工艺开发方法,通过提供对产品和工艺设计的更好理解,确保一致的产品质量。
PAT 应用在连续工艺中的关键要素是能够收集 CQA 信息并触发及时响应,以促进控制。分析测量必须在促进实时决策所需的时间范围内可用。此外,为了轻松实施 PAT 工具,仪器所需的成本不应该很高,至少在它不会大幅增加生物制药生产成本之前是这样。此外,选择的分析技术必须精确、准确和稳健。虽然连续工艺可从 PAT 实施中获得很多收益,但这些类型的工具还没有被充分探索过,并且针对连续工艺的发展,传感器技术、配置和稳健性仍需要重大改进。
关于上游工艺,经典过程传感器提供有关工艺变量的信息,例如温度、pH、溶解气体和泡沫水平。然而,涉及光谱传感器的、更强大的技术已成功用于过程监控。例如,近红外光谱已被最广泛地研究,以用于确定细胞培养液中单个成分的浓度,如 Arnold 等人所证明的那样。此外,拉曼光谱不仅可用于分析培养液成分谱,还可以用于监测蛋白质的结构/化学变化,尤其是用于在线监测聚体形成或糖基化等质量属性。最近,基于液相色谱-质谱的多属性方法已成为一种重要的 PAT,允许同时监测产品质量属性,如聚糖谱、电荷异构体和生物治疗药物的纯度。通过开发一个平台,从生物反应器中收集无细胞样品,然后使用自动液体处理系统进行自动高通量纯化,Dong 等人(2016)证明可以产生“近乎实时”的测量,为使用此类技术在整个生物生产过程中监测多个 CQA 奠定了坚实的基础。
对于下游工艺,PAT 的实施仍然相当有限,部分原因是缺乏传感器选项:pH、电导率、吸光度和压力传感器实际上并不能测量生物分子的质量属性,例如蛋白质聚集。然而,Kamga 等人 (2013) 采用多波长紫外光谱来有效地确定蛋白质混合物中单个成分的浓度,准确预测相对于目的蛋白质的聚体浓度。此外,对于层析步骤,实施 PAT 可能具有挑战性,因为这些单元操作的典型工艺时间很短。Sharma等人 (2006) 证明,通过在线分析型 LC,可以实现对层析步骤的连续监测,以发现聚集峰。使用在线高效液相色谱 (HPLC) 系统研究工艺层析柱的实时合并,并对其编程,以在聚集峰开始时停止收集,结果显示,使用 PAT,可促进基于产品质量属性的层析柱合并的实时决策。
因此,在连续工艺中,PAT 工具必须为后续的工艺步骤在线提供决定性信息,从而使工艺的连续性成为可能。未来,这些 PAT 的开发和实施将允许设计生产工艺,从而提供一致的、明确定义的优质产品并提高工艺效率。可预见的挑战包括实施非侵入过程监测技术,以及将先进传感器整合到自动化过程控制策略中。
数据采集/建模
生物技术行业中的生物工艺存在许多挑战,并且通常不如其它行业那么简单。操作的复杂性,尤其是发酵的复杂性,使该行业多年来一直处于“试错-优化”模式。然而,近年来,随着 QbD 和 PAT 的应用,人们对更好地理解这一工艺有了更大的推动。这使科学家和工程师能够对每个操作拥有更多的知识和细节了解,而不是将工艺纯粹视为“黑匣子”。将一个工艺(无论是发酵等相对复杂的过程,还是混合罐等更简单的过程)转化为数学模型的能力不仅可以加深对工艺的理解,还可以减少优化所需的时间和实验数量。机械模型 (MM) 旨在准确描述要描述的系统的物理化学现象,并且行业已经针对生物工艺发布了几个此类模型的示例。除了纯粹的机械模型之外,使用 MM 和机器学习的混合方法(如人工神经网络)可以帮助减轻计算机上的计算负载,例如,通过使用数据集来确定某些参数,然后将其用作模型的输入。这加速了工艺开发并提供了更快的结果,如文献中所示,用于估计工艺参数和优化整个下游工艺。一旦对此类模型进行了调整和训练,这些计算的输出将为工艺提供非常有价值的见解。很明显,无论是在工艺开发阶段还是在生产工厂中实施此类工艺后,模型对于向集成式连续生物生产的飞跃都非常重要。然而,建模不能完全脱离实验工作和数据。它需要数据来估计参数、训练模型并最终验证它们。此外,数学模型对于急需的控制策略的实施和实现非常重要,这对于确保如此复杂的生产线的正常运行至关重要。
模型的使用现在被工业界广泛接受,并且肯定是未来连续工艺的一个关键特征。行业需要能够根据基于准确描述的模型对工艺的意外变化做出动态决策的能力。这也提出了对可靠和准确数据收集的需求。再加上日益改进的传感器,非常需要快速且准确的分析,不仅收集有关工艺行为的数据,以便快速采取行动,而且能够监测和控制 CQA,并维护最终产品质量。考虑到生产工厂中发生的所有单元操作和过程,生成的数据量可能是巨大的。尽管生成的大量数据对于工艺理解和监控至关重要,但数据分析的自动化也同样至关重要。集成式连续生物生产倡议渴望找到方法来容纳和充分利用所有生成的数据,无论是用于工艺控制、工艺概览还是工艺开发。
上游/下游工艺连接
对于真正集成的连续生物生产,连续单元操作(上游和下游)的不间断连接是必要的,它们之间没有或很少发生隔离的中间性保持步骤。
行业已经建立了几个将连续上游工艺与捕获步骤相结合的例子,使用灌流培养技术从生物反应器中连续去除培养基和细胞外产物。整合这两个工艺步骤的一个主要挑战是使上游灌流流速与下游纯化流速同步。上游和下游系统之间的同步控制系统目前也较缺乏。因此,下游系统(前馈控制)不会检测到上游工艺的偏差,反之亦然(反馈控制)。这种类型的系统需要进一步的开发和测试,因为多个上游参数会影响后续的下游操作。Karst等人证明了通过安装近线 HPLC 来实施反馈控制的可能性,以提供生物反应器收获液的滴度数据,以调节捕获步骤的操作条件并通过使用控制回路调节连续体积流速。
尽管连续上游生物工艺已经相当完善,但完全连续的下游工艺的整合仍然是一个待开发领域。对于连续捕获和精纯层析,可以应用两个主要系统:周期性逆流层析 (PCC) 和模拟移动床层析。在真正集成的连续层析平台中,可以通过调节层析柱中的保留时间超过连续的柱步骤来实现工艺同步。为确保来自一根层析柱的劣质洗脱液材料不会与下一个功能性层析柱的材料混合,需要实时监测和反馈控制。柱之间的合并也可能引入交叉污染的风险,而反馈控制策略可能能够检测到流出液并将流出液从第二根柱转移。
Gomis-Fons等人(2019)在小规模条件下开发了不同层析柱和用于纯化重组蛋白的超滤单元之间的连接。外部控制器 Orbit 用于使系统自动化,并应用了开环和闭环控制策略:例如,入线监测 UV,并使用基于吸光度水平的自动产品合并。此外,在集成的连续下游工艺中,耗材需求(如层析填料和缓冲液消耗)的显著减少将导致运营成本的大幅降低。Gjoka等人 (2017) 将4个纯化单元操作转换为连续工艺,与相应的批次工艺过程相比,分别减少了 95% 和 44% 以上所需的填料和缓冲液体积,并显著降低了耗材消耗。因此,一个完全集成的连续工艺有可能优化质量、成本、速度和灵活性,最紧迫的挑战是为整个生物生产过程创建一个全局性的监测和控制策略。这不仅需要监测和控制所有入口和出口液流的连续测量(PAT 框架),还需要可现实的反馈和前馈控制策略,以确保最终产品质量。到目前为止,据作者所知,生产过程中的完整端到端集成仍有待开发。然而,Godawat 等人(2015) 已能够将灌流生物反应器与两个周期性 PCC 单元相结合,用于初始捕获和连续的离子交换步骤,表明创建完全集成的端到端连续生物工艺平台是可行的。最近,Coolbaugh 等人(2021)通过在中试规模上进行的成功概念证明,证明了这种端到端的连续工艺是可放大的。
其它需求
前文所述需求代表了需要进一步开发的三大领域。然而,也有一些需求完全没有得到关注,而另一些需求尽管没有完全被忽视,但仍然缺乏作为可靠解决方案的实用和/或可负担的技术。高通量筛选 (HTS) 日益普及,导致世界各地的工厂采用更自动化的实验室和小型化分析。长期以来,自动化液体处理系统的使用已被确立为 HTPD 在下游(主要是层析)中的标准,已经有报道描述了测定吸附等温线甚至完整层析运行的方法。使用此类设备可以实现检测的自动化,同时保持低使用量,从而实现更快、更具成本效益的分析。对于上游来说,HTPD 已经有了解决方案,但是,这些解决方案通常带有非常高的价格标签,例如 Ambr®系统,这可能会阻碍科学家和行业公司对此进行的投资。因此,该行业正在呼吁寻找负担得起的替代品,并认为微流体是满足这一需求的好机会。在细胞系开发方面,目前对于没有 Ambr® 系统的公司来说,最先进的技术是以批次模式获取性能更好的细胞株,然后在灌流模式下对其进行测试。因此,需要对细胞生物学有更深入的了解,这最终将推动以可承受的价格开发出更好的细胞系,而微流控技术将提供这一点。
微流控已被证明是一种强大的规模缩小模型,能够模拟多个单元操作,其优势在于使用更少的样本量并实现更快的分析。这些设备仍需要为在工艺开发中的应用铺平道路,但在结晶、层析、细胞培养、水双相系统、生物催化等不同的单元操作中已经显示出有希望的结果,并且已作为 HTS 设备的有希望的缩小模型。然而,过滤仍缺乏允许实现特定单元操作 HTPD 的规模缩小模型。膜过滤在微流体中也没有广泛使用。液体处理站对这种单元操作的 HTPD 的适应仍处于非常早期的阶段。过滤工艺开发通常需要大量的材料和耗时的工作。在这样的系统中使用 HTS 设备可减少工艺开发中的试剂消耗,同时避免设备尺寸过大,后者往往是工艺了解较差的结果。
结论
向连续工艺的转变是成熟行业的自然路径,生物制药行业正在其它行业的步伐,技术进步越来越多地推动了这种转变。这项技术的优点是巨大的,并且得到了很好的证明,即其可以在不同的规模上降低工艺成本,即使在不同的生产规模条件下,与最成熟的批次模式相比,也是如此。
通常,连续工艺允许实现更高效的工艺,同时降低占用空间。由于设备的使用效率更高,增加体积流速意味着连续工艺的设备和耗材成本的增加比批次工艺中观察到的要小。与连续生物工艺相对应的是对快速分析和控制的需求增加,这可以对操作条件的波动提供实时响应,以保证产品质量。
尽管过去 20 年的技术突破是巨大的,但我们可以理解,学术界和工业界都渴望更好的工艺技术。从研讨会的结果可以得出结论,虽然工艺开发和优化有很多选择,但改进的空间仍然很大,要么拥有新技术,要么找到降低现有技术价格的方法,以使工艺开发“民主化”。被认为最有希望填补 ICB 当前空白的工具包括建模和微/纳米流体。这符合监管机构在 PAT 和 QbD 倡议中的当前要求,其中更高的过程理解是为了实现对最终产品质量的控制,从而降低产品差异,满足CQA。
上游和下游工艺研究的最新进展允许实现以连续模式运行具有竞争力的单元操作,从而使这些新工艺优于先前建立的工艺。由于多年来上游和下游工艺是分开开发的,现在的挑战在于将所有这些单元操作集成到一个连续的端到端生产过程中。软件和硬件的集成对于实现完全连续的工艺流程以及前馈和反馈的工艺控制非常重要,以便根据其它单元操作中发生的情况做出更快的决策。PAT 的进一步发展和控制系统的同步化将是生物制药行业向端到端连续工艺转变的关键推动力。
缩短上市时间通常会阻碍连续工艺的实施,因为更容易“安全行事”并确保“赢得比赛”。然而,生物仿制药可以利用专利到期并押注这种工艺模式,旨在实现更高效、更便宜的工艺,使生物仿制药生产公司能够与其它参与者竞争。
原文:M.N.Sao Pedro, T.C.Silva, R.Patil, et al., White paper on high‐throughput process development for integrated continuous biomanufacturing. Biotechnology and Bioengineering, 2021, DOI: 10.1002/bit.27757.






