近几十年来的研究创新为 mRNA 作为新兴疫苗技术的发展奠定了基础。与传统疫苗平台相比,基于 mRNA 的疫苗开发相对于其它类型疫苗的加速得益于其简单的生产过程和安全性。首先,mRNA 不构成插入诱变的风险。它是非感染性的,并在细胞内自然降解。其次,可以通过修饰和各种递送方法使 mRNA 更加稳定,使其在宿主细胞中高效且易于翻译。此外,可以使用体外转录 (IVT) 反应在无细胞系统中制备 mRNA,与传统的基于细胞的疫苗平台相比,该技术更易于生产和调节。最后,mRNA 生产可以应用于使用类似生物过程的各种抗原,使该技术易于适应和更加通用。
最近的 COVID-19 大流行凸显了拥有随时可用的疫苗平台以应对新兴流行病的重要性。为了应对大流行,mRNA 技术是第一个作为 COVID-19 治疗药物进入I期临床试验的候选疫苗,疫苗的临床试验在序列鉴定后两个月开始。因此,mRNA 技术被带到了疫苗疗法研究和开发的前沿。强调使用 mRNA 疫苗治疗当前和新出现的疾病的前瞻性研究已经推动许多候选疫苗进入各种传染病的临床试验。因此,由于新型 mRNA 疫苗技术带来的好处和灵活性,人们越来越有兴趣在未来几年推进其工业规模生产。这将涉及增强和优化 mRNA 生物工艺,以适应各种抗原平台。
本综述将概述 mRNA 疫苗的设计和 mRNA 疫苗平台的当前技术发展。此外,文章将侧重于疫苗设计、生产和当前实施的关键质量属性范例,以实现高规格 mRNA 疫苗生产的创新。最后,将讨论 PAT 集成的生物制药生产的未来方向和发展。
作为疫苗的 mRNA 的进化
1989 年,一项开创性的研究证明了使用脂质体进行 RNA 转染可生产蛋白质。不久之后,另一项研究表明,将裸露的 mRNA 注入小鼠肌肉细胞会导致编码蛋白在体内表达。这些研究确立了使用体外转录的 mRNA 在细胞内生产蛋白质的可行性。然而,尽管有这些有希望的发现,但由于对 mRNA 稳定性和翻译效率的担忧,使用 RNA 作为治疗工具面临着几个重大挑战。因此,它并没有立即被认为是一种可行的治疗选择。
直到 2000 年代初,修饰核苷酸的技术突破和递送方法的进步才为 mRNA 作为潜在治疗药物铺平了道路。许多创新,例如使用修饰的核苷酸、特定密码子序列以及使用高效液相色谱 (HPLC) 消除双链 RNA 污染物,有助于提高 mRNA 的稳定性,并减轻不需要的免疫原性反应,从而推动了 mRNA 疫苗的开发。此外,细胞质 mRNA 递送的效率也因各种递送方法而发生了革命性变化,包括使用脂质纳米颗粒 (LNP)。
mRNA抗原的类型
通过体外转录 (IVT) 产生的 mRNA 抗原的结构与成熟的真核 mRNA 非常相似。它们包含一个编码目标抗原的开放阅读框 (ORF),两侧是 5' 和 3' 非翻译区 (UTR) 和一个 5' 引物帽结构,以及一个 3' poly(A) 尾部。目前,已经评估了两种类型的 mRNA 抗原构建体:非复制和自我扩增的 mRNA 抗原。两者的结构相似,除了自我复制型 mRNA 还包括通常来自单链 RNA 病毒的病毒复制酶基因(图 1)。非复制性 mRNA 抗原由于其 RNA 长度较短和直接抗原表达而更容易生产。然而,由于其表达时间较短,它可能需要更高的剂量才能产生适当的免疫反应。自扩增 mRNA 抗原可以缓解这个问题,因为它携带病毒复制酶基因,以增强 mRNA 表达持续时间。然而,由于较长的 RNA 转录本长度和自我扩增的潜在免疫反应,目前在生产和优化此类抗原方面仍存在挑战。研究人员目前正在探索优化 mRNA 抗原表达和稳定性的策略。
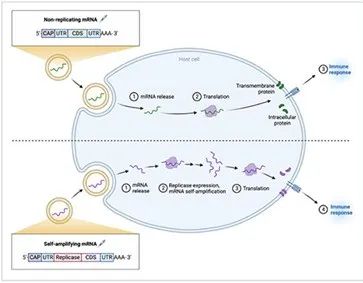
图1:使用非复制mRNA和自扩增mRNA表达抗原的简化示意图。同样,非复制和自我扩增的RNA都可以用脂质纳米颗粒 (LNP) 包裹,以促进细胞摄取,并防止mRNA降解。非复制的mRNA结构体在细胞质中被翻译,以产生目的蛋白质,此外,自扩增的mRNA也被翻译,以产生复制酶机制,用于扩增目标蛋白质。所得抗原蛋白以跨膜或细胞内蛋白的形式产生,用于刺激免疫反应。
优化 mRNA 抗原效率
设计有效的 mRNA 候选疫苗需要仔细考虑许多工艺属性。最近的进展创造了改造 mRNA 技术以创造更适合的 mRNA 疫苗抗原的机会。对于 mRNA 疫苗,有两个主要成分:mRNA(抗原)(图 2)和脂质纳米颗粒(递送系统)。这两个组成部分都需要进行监管,以确保高质量的疫苗生产。
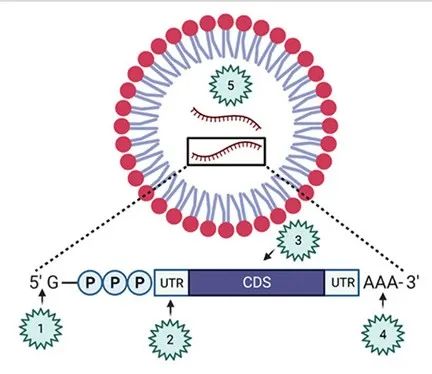
图2:mRNA抗原设计的关键质量属性。影响转录质量、效率和稳定性的mRNA抗原属性包括[1]5' 帽、[2]非翻译区、[3]编码序列、[4]3' Poly(A) 尾、[5]mRNA纯度。
mRNA 5'帽:该帽是mRNA抗原的重要组成部分,在调节翻译起始和免疫原性中起重要作用。有两种常见的帽状结构:cap O,由甲基-7鸟嘌呤核苷酸通过5'三磷酸连接到5' 位置;cap 1,涉及核糖2'-O位置的mRNA首核苷酸甲基化。这些帽通过防止外切酶降解来稳定mRNA转录物,并提供有效的翻译起始位点来招募核糖体。此外,加帽mRNA有助于防止先天免疫反应的过度激活。有几种方法可以将5'帽添加到mRNA转录物上。一种方法是在IVT反应中使用合成的帽类似物,而另一种方法涉及使用CleanCap®方法将cap 1结构添加到特定的转录起始序列。加帽也可以使用牛痘加帽系统作为酶促反应来完成。这些方法确保了对mRNA抗原的有效和精确的5'加帽,这对于开发有效的疫苗至关重要。
mRNA 5'和3'非翻译区(UTR's):5'和3'非翻译区分别对翻译效率和mRNA稳定性至关重要。优化的序列特异性富集UTR可以通过影响翻译机器识别、招募和mRNA运输来促进蛋白质产量。优化可以通过调整3'和5' UTR的长度来实现,或者使用特定的核苷酸富集 (例如,5' UTR Kozak序列用于翻译效率,3' UTR au丰富元件用于调节转录物稳定性)。选择基于其它天然稳定表达较长的mRNA分子的UTR也有助于提高mRNA的翻译效率和转录物的稳定性。
抗原编码序列:为了丰富抗原表达,目前使用密码子优化和组成来提高转录效率(如GC含量)。此外,修饰的核苷酸,包括甲基化核苷和假尿嘧啶,可以帮助保护mRNA免受强烈的免疫刺激反应,增加mRNA的稳定性,允许更长的转录物表达,并提高疫苗的安全性。
mRNA 3' Poly(A) 尾:3' Poly(A) 尾通过保护序列免受核酸酶降解和为Poly(A) 结合蛋白结合提供位点,对mRNA的稳定性很重要。Poly(A) 尾的最佳长度取决于细胞类型,必须仔细优化以提供最大的稳定性。研究表明,poly(A) 尾的长度与mRNA表达的持续时间之间存在相关性。添加poly(A) 尾的主要方法有两种。第一种方法是将poly(A) 编码序列直接添加到用于IVT的DNA模板中。第二种是使用单独的酶促反应,利用聚A聚合酶。poly (A) 尾的优化对于确保mRNA转录物保持完整和功能至关重要,从而提供安全有效的候选疫苗。
mRNA纯度:mRNA纯度是一项关键的质量属性,必须仔细控制,以确保疫苗效力和最佳免疫反应。RNA污染物激活触发mRNA降解和抑制翻译的免疫反应。dsRNA污染物是IVT期间异常聚合酶活性产生的杂质的一种形式。为了减轻这种情况的发生,使用HPLC纯化IVT mRNA有助于去除dsRNA,增加蛋白质产量,同时减少不必要的免疫激活。
脂质纳米颗粒 (LNP) 递送mRNA疫苗的优化:为了确保mRNA疫苗的有效性,需要将抗原正确递送到细胞中,以表达目的蛋白质。虽然裸mRNA可以在不同的细胞类型中整合和表达,但最佳表达需要一种递送机制。这不仅有助于正确地递送mRNA,以产生抗原,而且还保护其免受核酸酶的降解。在各种递送系统中,目前LNP已广泛用于疫苗开发,包括COVID-19 mRNA疫苗。大多数LNP配方含有阳离子或电离脂质以及磷脂、胆固醇和聚乙二醇(PEG)脂质。每种类型的脂质在调节细胞细胞质中mRNA抗原颗粒的稳定性、有效性和生物分布方面发挥着不同的作用,可电离脂质有助于内体从中性pH值转换为酸性pH值,这对于细胞摄取后mRNA的释放很重要。其它脂质,包括磷脂,如1,2-二硬脂酰-sn-甘油-3磷脂胆碱 (DSC)和DOPE,有助于稳定LNP结构,并有助于脂质纳米颗粒的内体释放。此外,胆固醇促进LNP结构的完整性,从而促进细胞有效摄取。最后,聚乙二醇化脂质通过延长纳米颗粒在血液中的循环,以促进细胞摄取和减少聚集,从而增强LNP的稳定性。因此,mRNA和LNP递送系统的属性和成分在mRNA疫苗产品的生产过程中是调节和控制抗原产量和质量的关键考虑因素。
mRNA生产的演变和未来展望
mRNA疫苗生产概述
目前的mRNA生产过程可分为三个不同的阶段:1- mRNA活性物质的生产,2- RNA-LNP的配制,3-终产品的生产。
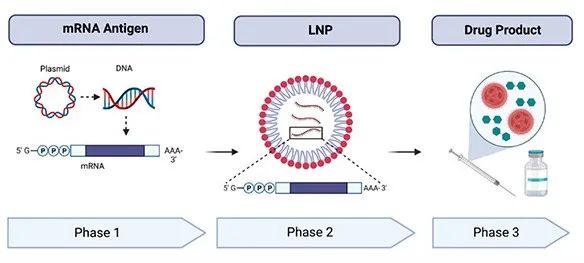
图3:mRNA疫苗生产的主要工艺阶段概述:1-mRNA活性物质的生产,2-RNA-脂质纳米颗粒的制剂,3-终产品的生产。
阶段 1: mRNA 活性物质的产生
上游 mRNA 平台过程通常涉及使用大肠杆菌发酵从质粒中产生 DNA 模板。使用限制性内切酶将质粒线性化并用于 IVT 反应,其中包含 NTP、缓冲液、MgCl2 以及 T7、SP6 或 T3 RNA 聚合酶,以在体外转录 mRNA。转录后修饰,包括 5' 加帽和 3' Poly (A) 尾添加,通常在 mRNA 合成后进行。使用 DNase 消化任何剩余的 DNA 模板。当前使用 CleanCap® 或帽类似物的加帽技术创新可以简化反应过程,并在 IVT 反应期间完成 5' 加帽,同时添加由模板 DNA 编码的 Poly(A) 尾。
IVT 反应后,必须从反应混合物中纯化 mRNA,因为许多杂质包括酶、残留的 NTP、残留的 DNA 和来自提前中止反应的短 RNA,而双链 RNA (dsRNA) 会刺激不需要的免疫反应并降低产品安全性。虽然目前还没有基于法规要求的标准化纯化方法,但目前各种mRNA抗原平台采用多种纯化和过滤方法。纯化技术,例如尺寸排阻层析 (SEC)、离子对反相层析 (IPC)、离子交换层析 (IEC)、脱氧胸苷 (dT) – Oligo dT 亲和层析、羟基磷灰石或疏水相互作用、多模式或基于纤维素的层析法。此外,切向流过滤 (TFF) 也可用于去除杂质,同时进行浓缩和溶液洗滤,使其成为大规模生产的通用过滤方法。 TFF 通常与 mRNA 沉淀结合使用,这样可以保留 mRNA,同时通过洗滤去除杂质。常见的 IVT 纯化方案通常结合使用 TFF,然后是层析步骤和第二个 TFF,以正确纯化 mRNA,去除工艺污染物,并促进浓缩和缓冲液置换。
阶段 2 和 3: RNA-LNP 的配制和终产品生产
mRNA产物制备完成后,进行LNP配制和包封,组装疫苗抗原。这是通过使用微流控或基于喷射的快速混合技术,将在水性缓冲液中的 mRNA 和在乙醇中的脂质混合来实现的。然后使用 TFF 和除菌过滤纯化载有 mRNA 的 LNP,用于第3阶段的最终灌装。在此阶段,将除菌过滤和稀释的 mRNA 疫苗添加到适当的小瓶中,加盖并密封,以进行最终药物产品包装。
mRNA 疫苗质量源于设计 (QBD) 框架
要为 mRNA 疫苗设计有效的生产工艺,重要的是定义关键质量属性 (CQA) 并了解生产高质量抗原所需的检测类型。这种方法可以提供一个路线图,根据有关当前生产疫苗的技术和监管要求的先验知识来优化生产实践,以调节 mRNA 抗原的质量,确保产品的效率、效力和安全性以及预期的免疫效果。
从 mRNA 疫苗活性物质到最终药物产品,需要考虑各种 COA。例如,与 dsRNA 和 mRNA 结构元素(包括 5' 帽和 3' poly-(A) 尾)相关的质量属性对于检测和调节很重要,因为它们会影响细胞免疫反应、翻译效率和转录本稳定性。同样,对于 LNP 配制,了解颗粒大小、电荷和脂质含量对于优化药物产品功效和细胞免疫反应至关重要。因此,生产框架的设计需要整合质量属性和预期质量结果,以确定在整个生产过程中监控所需的 CQA。
mRNA 疫苗的生产工艺设计需要全面了解质量属性和关键工艺参数之间的关系,以确保最终药品的质量。首先要了解 mRNA 疫苗设计、可能影响疫苗质量的上游和下游工艺。例如,加帽机制等上游工艺可能需要额外的纯化步骤,这可能会影响抗原产量。监测 IVT 反应时间和温度有助于优化 mRNA 产量,同时保持转录本的质量。检测这些参数对于确保 mRNA 疫苗抗原质量,以避免产品杂质(包括 dsRNA 颗粒污染物)非常重要。
下游工艺对于防止 mRNA 变性和沉淀很重要。例如,需要优化与 TFF 结合的商业规模层析方法的选择,以确定 RNA 截留和纯化的最佳条件,同时保持 mRNA 质量。此外,LNP 形成技术(包括混合率)会影响 mRNA 封装和 LNP 颗粒完整性。目前,由于纯化技术和表征工具之间缺乏明确的调节或优化方法来监测抗原产量,因此 mRNA 生产仍然存在许多未知的关键工艺参数。因此,有必要开发过程分析技术 (PAT) 解决方案,以更好地了解过程参数,确保最终产品的质量和纯度。
用于 mRNA 生产的 PAT 和数字设计框架
为了连接关键质量属性和过程控制,可以使用 PAT 开发分析工具。 PAT 使用数据模型创建工具,为工艺优化提供有关质量属性的更多信息,并提供实时监控生物过程的解决方案,从而实现预测控制和过程自动化。目前,有许多离线技术被用于表征基于 mRNA 的疫苗的工艺参数,包括有关 mRNA 产量、回收率、总含量和结构完整性的信息。然而,有关 mRNA 序列、5' 帽、Poly(A) 尾长度和 RNA 纯度的质量属性仍需要额外检测。此外,有关药品纯度的信息,包括来自大肠杆菌 DNA 模板生产的 dsRNA 污染物、残留 DNA、酶和蛋白质,对于确保用于封装的适当 mRNA 抗原溶液也很重要。最后,mRNA-LNP 颗粒的特征对于表征很重要,包括 RNA 封装、LNP 大小、稳定性、电荷、形态、脂质含量和杂质,以确保疫苗将被有效和正确地包装,以实现适当的细胞摄取。因此,质量源于设计 (QBD) 和 PAT 框架的目的和目标是设计能够使用可适用于数字化建模和实时反馈的分析工具测量所有重要工艺参数和质量属性的过程。
已经开发了各种 PAT 工具来在 mRNA 疫苗生产过程中实时测量 CQA。例如,可以集成 UV-VIS 光谱法或自动通量圆二色性 (CD) 来监测 RNA 完整性和杂质。紫外光谱可以应用到可用于测量 RNA 浓度的在线技术中。另一方面,CD 可用于测量 RNA 二级结构。在线动态光散射 (DLS) 可用于在下游纯化过程步骤中测量 LNP 粒径分布。包括核磁共振 (NMR) 在内的其它分析技术可用于实时监测,以识别脂质并量化脂质降解和其它特征,包括纳米颗粒结构完整性。这些示例共同强调了开发 PAT 工具的必要性,这些工具可用于实时过程中监控 mRNA 关键质量属性,以更好地理解和控制 mRNA 生产过程。
结论
对 mRNA 疫苗的需求不断增加,需要标准化的方法和监管框架。它创造了对方法创新的需求,以更好地理解和测量 mRNA 疫苗产量、质量和安全概况所需的质量属性。可以使用类似生产工艺调整 mRNA 抗原的多功能性,为开发可应用于未来 mRNA 疫苗抗原平台数字生产的 QBD 框架和模型提供了极好的机会。本文中概述的分析工具的开发将有助于提高对上游和下游 mRNA 生产过程的了解。这提供了一个框架来帮助转移工艺知识,这些知识可以针对新的疫苗抗原平台进行调整和扩展。此外,PAT 工具的开发推进了工艺的数字化,并允许过程反馈控制,以优化 mRNA 疫苗生产流程。
原文:G.Gerzon, Y.Sheng, M.Kirkitadze, Landscape of mRNA vaccine design and manufacturing technologies. Biopharma-Asia, 2023.






